CP-1® High Grade 技術情報
造血幹細胞用 細胞凍結保存液
本製品は、1992年から販売しているCP-1の後継品です。
CP-1は造血幹細胞の凍害保護を目的として、Hydroxyethyl starch(HES)とDMSOの混合液を用いた、プログラムフリーザーを使用しない-80℃での簡易凍結法の試薬として開発されました。1992年の発売以来、多数の論文報告があります。造血幹細胞だけでなく、間葉系幹細胞、iPS細胞など様々な細胞を安定して凍結保存できることを確認しています。
特徴
- 再生医療等製品材料適格性確認済み※1
- 原薬等登録原簿(MF)登録済み
- 国内の弊社GMP対応施設にて製造
- 非臨床安全性試験実施済み
- USPグレードのDMSO使用
- 動物由来原料 不含
- 組成を開示
- 無菌試験、エンドトキシン、マイコプラズマ否定試験を実施
- 最終DMSO濃度は5%
※1 再生医療等製品の材料として生物由来原料基準等の適格性を満たしていることをPMDAに確認いただいています
| 製品コード | 製品名 | 用途 | 容量 | 貯法 | 希望小売価格 |
|---|---|---|---|---|---|
| 27207 | CP-1® High Grade | 造血幹細胞、間葉系幹細胞、 その他細胞の凍害保護液 |
50 mL×2 | 室温 | ¥10,800 |
| 27206 | 100 mL×2 | ¥18,000 |
・間葉系幹細胞やその他細胞向けのリーフレットはこちら
・CP-1 High Gradeの詳細とアプリケーションデータを掲載:パンフレットはこちら
組成情報
- ヒドロキシエチルスターチ
- ジメチルスルホキシド
- 生理食塩水
CP-1® High Gradeで凍結可能な細胞例
| 付着系細胞 | |||
|---|---|---|---|
| ヒトiPS細胞 | PFX#9 | ヒトES細胞 | H9 |
| ヒト脂肪組織由来間葉系幹細胞 | MSC-AT | ヒト骨髄由来間葉系幹細胞 | MSC-BM |
| ヒト新生児由来皮膚繊維芽細胞 | NHDF-Neo | ヒト胎児腎臓由来細胞 | HEK293 |
| チャイニーズハムスター卵巣細胞 | CHO-K1 | ヒト骨芽細胞 | Human Osteobrast |
| 浮遊系細胞 | |
|---|---|
| マウスハイブリドーマ | SJK-287-38 |
| ヒト造血幹細胞 (ヒト末梢血幹細胞、ヒト臍帯血幹細胞、ヒト骨髄幹細胞) |
|
技術資料一覧はこちら
実例集
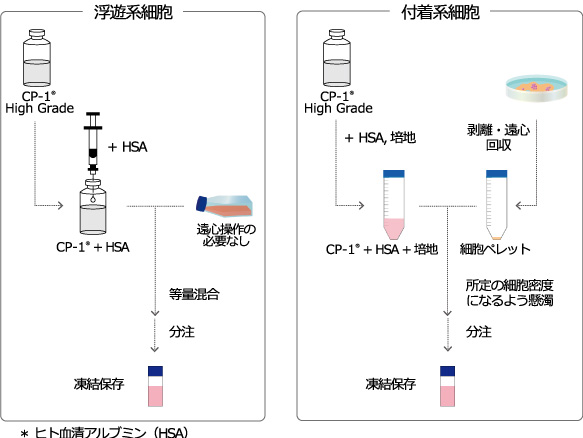
- Ⅰ.浮遊系細胞と付着系細胞の凍結方法
- Ⅱ.CP-1® High Gradeを用いた造血幹細胞の凍結保存・解凍方法
- Ⅲ.CP-1® High Gradeを用いた間葉系幹細胞の凍結保存・解凍方法
- Ⅳ.評価結果(間葉系幹細胞を用いた凍結保存 検討)
- Ⅴ.評価結果(組換えヒトアルブミン×間葉系幹細胞を用いた凍結保存 検討)
- Ⅵ.評価結果(iPS/ES細胞の凍結保存 検討1)
- Ⅶ.評価結果(iPS/ES細胞の凍結保存 検討2 ~凍結処理速度~)
- Ⅷ.評価結果(T細胞の凍結保存検討)
Ⅰ.浮遊系細胞と付着系細胞の凍結方法
Ⅱ.CP-1® High Gradeを用いた造血幹細胞の凍結保存・解凍方法
使用手順の詳細は “使用説明書” をご確認ください。
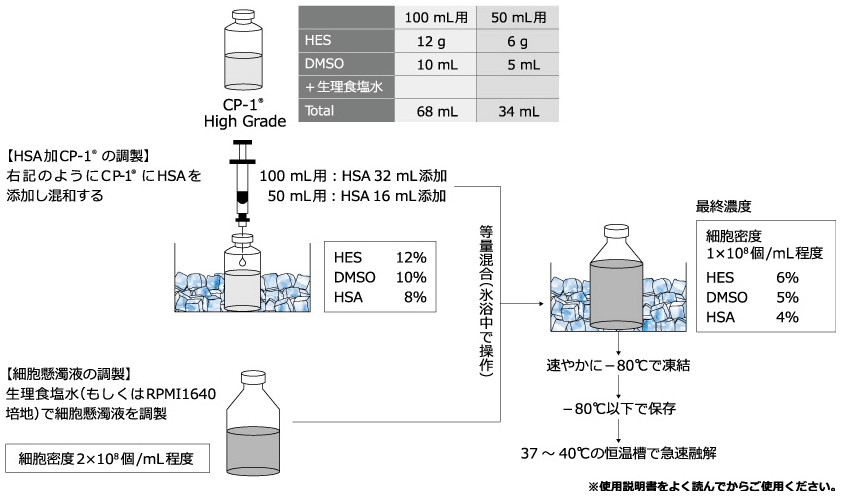
Ⅲ.CP-1® High Gradeを用いた間葉系幹細胞の凍結保存・解凍方法
手順の詳細は “ CP-1® High Gradeプロトコル集” をご確認ください。
凍結保存液の調製
- CP-1® High Grade, 25% HSA, 培地を4℃で冷やす。
- CP-1® High Grade 6.8 mL, 25%HSA 3.2 mL, 培地 10.0 mLを遠心管に加え、均一に混和する。
- 使用直前まで 4℃にて保管する。
細胞の凍結保存
- 凍結保存する細胞を剥離液などで回収し、細胞数を計数する。
- 遠心により上清を除去する。
- あらかじめ4℃に冷やしておいたCP-1® High Grade/25% HSA/培地(凍結保存液の調製-2)を加え、
1×106 cells/mLになるように均一に縣濁する。 - 1 mLずつクライオチューブに分注し、フリージングコンテナに入れ、-80℃で緩慢凍結する。
- 翌日に液体窒素または-150℃ディープフリーザーへ移す。
細胞の解凍
- あらかじめ培地9 mLを遠心管に準備しておく。
- 凍結していたクライオチューブを液体窒素から取り出し、37℃の温浴で急速解凍する。
- 解凍した細胞全量を培地へ加え、遠心する。
- 上清を除去し、適量の培地を加える。
- 使用する細胞種毎の最適な条件にて培養を行う。
Ⅳ.評価結果(間葉系幹細胞を用いた凍結保存 検討)
(兵庫医科大学 山原研一先生との共同研究、特許出願中)
【目的】 今後の再生医療への利用が期待されるヒト間葉系幹細胞(hMSC)について、CP-1® High Gradeで凍結保存し、安価かつ簡便なドライアイスで安定的に長期輸送が可能か検討した。
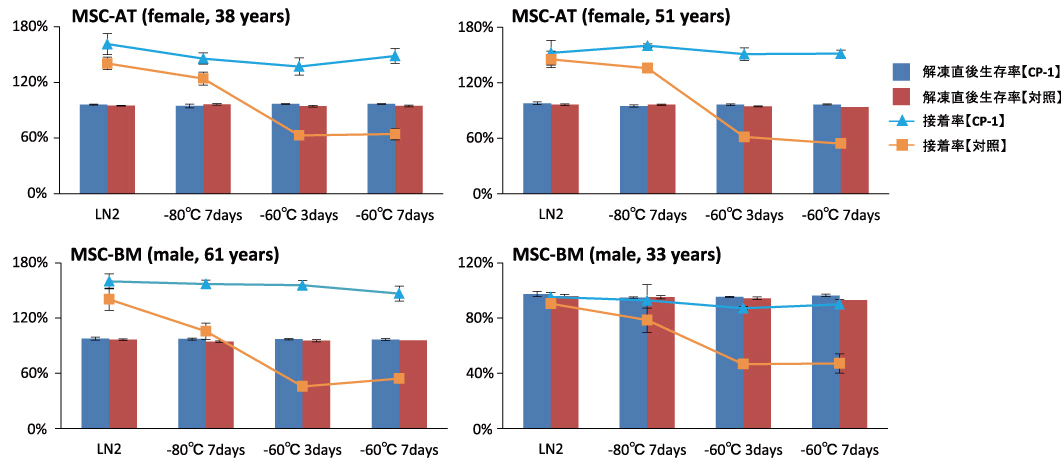
【方法】 ヒト脂肪由来間葉系幹細胞(MSC-AT)またはヒト骨髄由来間葉系幹細胞(MSC-BM)をCP-1® High Gradeもしくは対照(下図A)にて凍結し(1 x 106 cells/mL)、液体窒素タンクで保管した。液体窒素タンクで保管後、ドライアイス輸送を想定した各条件下で保管し(-80℃・7日間, -60℃・3日間, 60℃・7日間)、解凍直後の生存率および翌日の培養器への接着率を確認した(接着率=生細胞数/播種生細胞数)。
【結果】 全ての条件において、解凍直後の生存率は90%以上であり、差異は認められなかった(下図B)。しかし、対照で凍結したhMSCでは-60℃で保存すると解凍翌日に培養器へ接着しない死細胞が多数認められたが、CP-1で凍結したhMSCでは死細胞がほとんど認めらず、ほぼ全ての細胞が接着していた(下図B,C)。
【結論】 ドライアイスそのものの温度は約-80℃であることから、CP-1® High Gradeで凍結したhMSCはドライアイスを用いて安定的かつ長期的に輸送することが可能だと考える。
詳細はこちら:間葉系幹細胞への凍害保護液CP-1の利用(第18回日本再生医療学会ポスター発表)
A. 凍害保護液の組成

B. 解凍直後の生存率および翌日の接着率
C. 培養翌日の細胞の様子
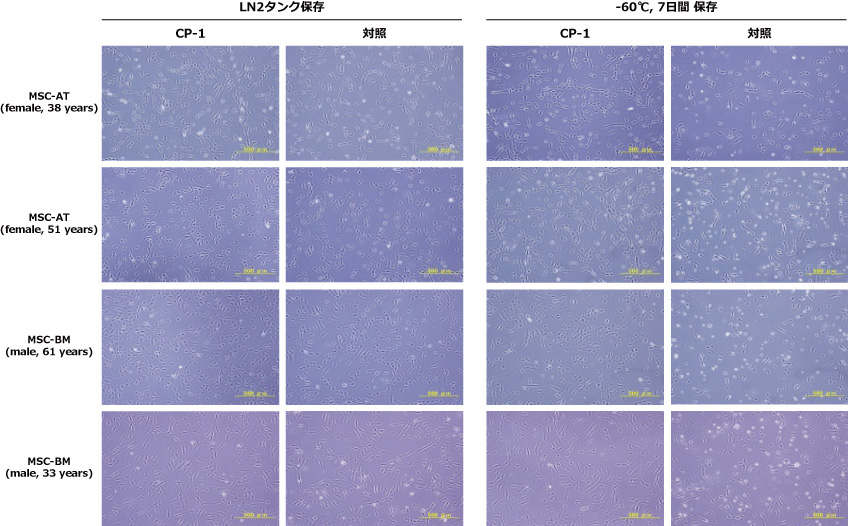
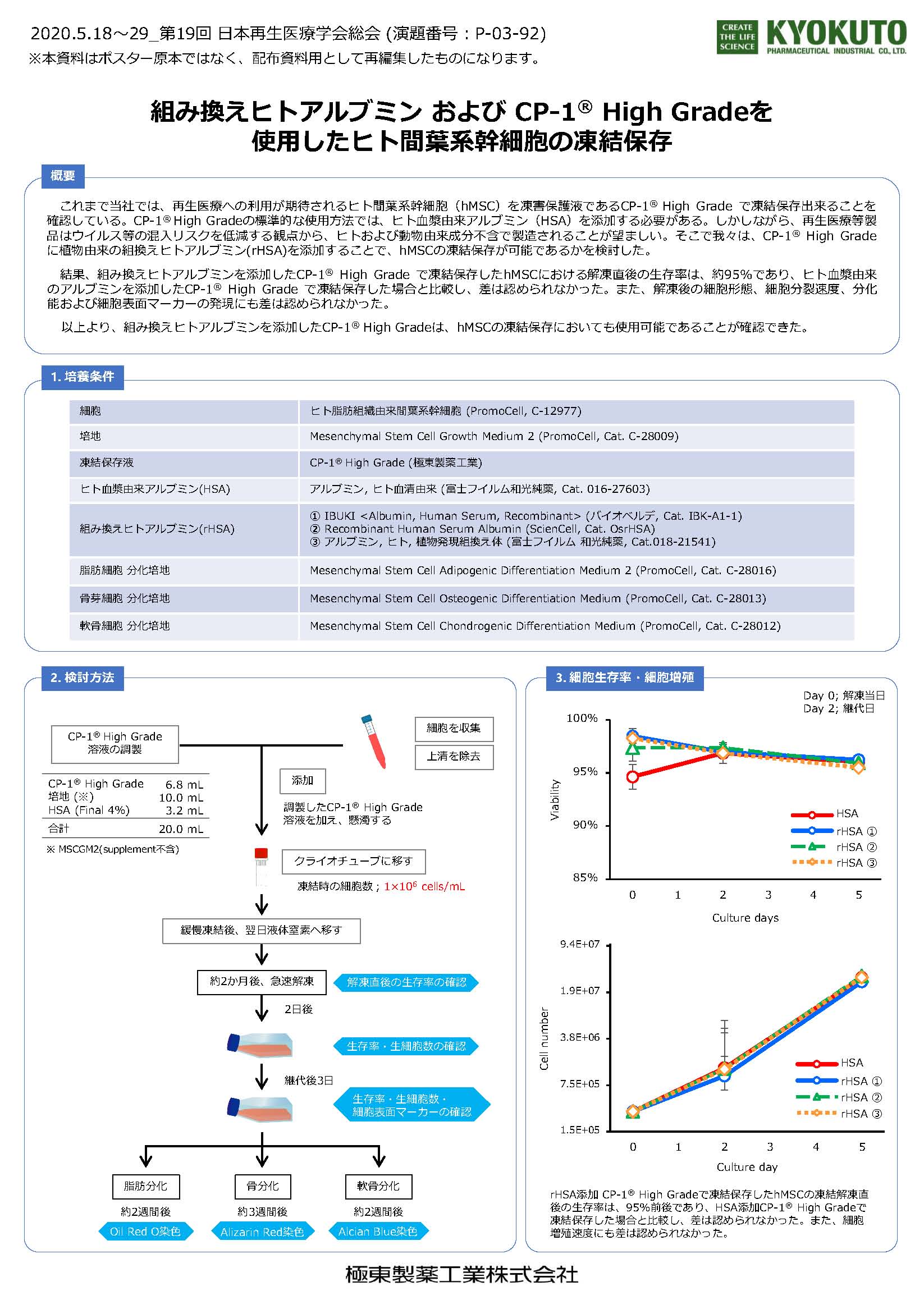
Ⅴ.評価結果(組換えヒトアルブミン×間葉系幹細胞を用いた凍結保存 検討)
(第19回 日本再生医療学会ポスター発表)
【概要】
これまで当社では、再生医療への利用が期待されるヒト間葉系幹細胞(hMSC)を凍害保護液であるCP-1®High Grade で凍結保存出来ることを確認している。CP-1® High Gradeの標準的な使用方法では、ヒト血漿由来アルブミン(HSA)を添加する必要がある。しかしながら、再生医療等製品はウイルス等の混入リスクを低減する観点から、ヒトおよび動物由来成分不含で製造されることが望ましい。そこで我々は、CP-1® High Gradeに植物由来の組換えヒトアルブミン(rHSA)を添加することで、hMSCの凍結保存が可能であるかを検討した。
結果、組み換えヒトアルブミンを添加したCP-1® High Grade で凍結保存したhMSCにおける解凍直後の生存率は、約95%であり、ヒト血漿由来のアルブミンを添加したCP-1® High Grade で凍結保存した場合と比較し、差は認められなかった。また、解凍後の細胞形態、細胞分裂速度、分化能および細胞表面マーカーの発現にも差は認められなかった。以上より、組み換えヒトアルブミンを添加したCP-1® High Gradeは、hMSCの凍結保存においても使用可能であることが確認できた。
詳細はこちら:rHSAとCP-1® High Grade を用いたhMSCの凍結保存(ポスター発表資料_再編集)
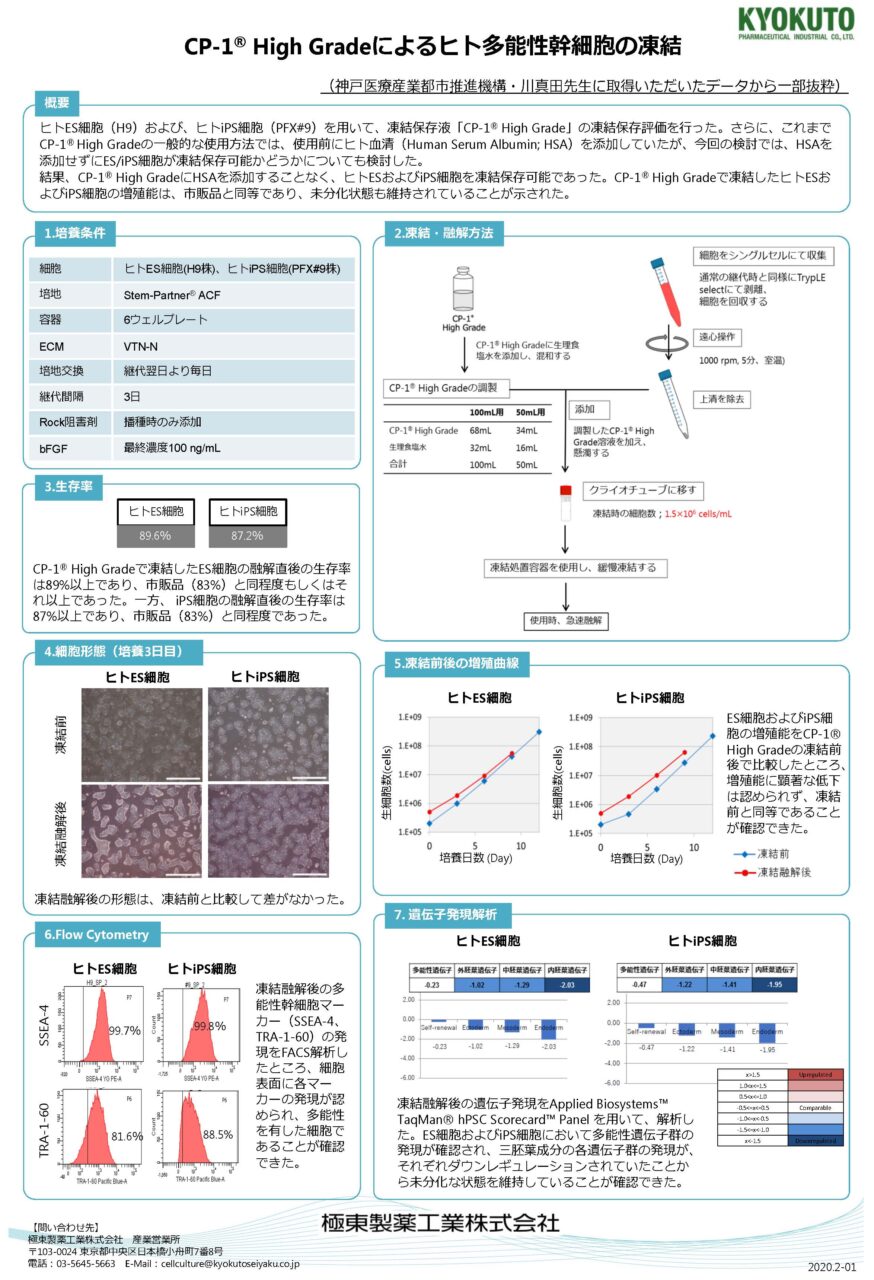
Ⅵ.評価結果(iPS/ES細胞の凍結保存 検討1)
(神戸医療産業都市推進機構(川真田先生)において取得いただいたデータを一部抜粋)
【概要】
CP-1®High Grade を用いてヒト多能性幹細胞を緩慢凍結できるかどうかを検討するため、CP-1®High Gradeで凍結保存したヒトiPS細胞またES細胞を解凍し、培養した際の増殖能および未分化状態を評価した。
またこれまでのCP-1®High Gradeの使用方法では、使用前にヒト血清(HSA)を添加していたが、HSAはヒト由来成分であるため添加しないことが求められる場合もある。そこで、今回の検討では、HSAを添加せずにiPS/ES細胞が凍結保存できるかについても検討した。本方法では、DMSOの最終濃度は10%になるように調整している。
結果、CP-1®High Gradeで凍結したiPS/ES細胞の増殖能は、市販品と同等であり、未分化状態も維持されていることが示された。つまりCP-1®High Gradeは、ヒト多能性幹細胞の凍結においても使用可能であることが確認できた。
詳細は こちら
Ⅶ.評価結果(iPS/ES細胞の凍結保存 検討2 ~凍結処理速度~)
(大阪大学大学院工学研究科 紀ノ岡研究室(福守先生ら)において取得いただいたデータ)
【概要】
ヒト人工多能性幹細胞(hiPSC)を凍害保護液であるCP-1® High Gradeで凍結保存できることを確認している。〔CP-1® High Grade 技術情報-実施例Ⅵ 参照〕
これまでに紹介したCP-1® High Gradeを用いたhiPSCの凍結保存方法では、凍結処理容器を使用し、-1℃/minに近い冷却速度での凍結保存を推奨している。しかしながら、一度に大量の細胞を凍結保存する際は凍結処理容器が不足すること、容器に入れる作業に手間がかかることなど課題があり、操作性の向上が求められていた。そこで、凍結処理速度が異なる条件にてhiPSCの凍結保存を行い、凍結解凍後の生細胞数比と接着率を確認した。
結果、-1℃/minに近い冷却速度(凍結処理容器を使用した場合)と、冷却速度を管理しない条件(凍結処理容器を使用していない場合)にて凍結保存したhiPSCの凍結解凍後の生細胞数比に差は認められなかった。また、解凍播種24時間後の細胞接着率は、凍結処理容器を使用していない条件よりも使用した条件のほうが良好であったが、いずれもhiPSCの凍結保存には十分な性能であると考えられえる。
以上より、CP-1® High Gradeは凍結処理容器を使用しない条件(冷却速度を管理しない状態)にてhiPSCを凍結保存可能であることが確認できた。
詳細は こちら

Ⅷ.評価結果(T細胞の凍結保存検討)
(当社取得データおよび神戸医療産業都市推進機構取得データを一部抜粋)
【概要】
近年の再生医療分野では、ヒト間葉系幹細胞(hMSC)やヒト人工多能性幹細胞(hiPSC)を用いた治療のほか、免疫細胞を用いた遺伝子治療や免疫細胞治療も盛んである。国内でも承認されているキメラ抗原受容体T細胞(CAR-T)療法などは、患者から採取した細胞に遺伝子導入し、免疫機能を活性化させた細胞を再び患者へ投与する。その場合、最終的に投与される遺伝子治療製品は細胞懸濁液となる。そのため、細胞の機能を保持したまま保存できる試薬が求められている。
凍害保護液であるCP-1® High Gradeは、造血幹細胞の凍結保存に広く使用されており、当社でもこれまでに造血幹細胞やhMSC、hiPSCを凍結保存できることを確認している〔本ページ参照〕。そこで今回は、今後の再生医療への利用が期待されている免疫細胞の一種である、 T細胞の凍結保存について検討した。
4種類の保存液を用い、ヒト末梢血単核球(hPBMCs)から活性化・拡大培養したT細胞を凍結保存した。その結果、検討した全ての保存液において、解凍直後の生存率は90%以上であり、HSA添加・非添加に関わらず保存可能であった。また、細胞形態は凍結保存前後で特に変化は認められなかった(社内検討より)。さらに、凍結前後における細胞表面マーカー発現においても、大きな変化は認められなかった(外部評価より)。
以上より、CP-1® High Gradeはヒト末梢血単核球(hPBMCs)から活性化したT細胞を凍結保存可能であることが確認できた。
詳細は こちら

参考資料
- CP-1使用文献一覧
- 間葉系幹細胞への凍害保護液CP-1の利用
(第18回日本再生医療学会ポスター発表) - 間葉系幹細胞への凍害保護液CP-1の保護効果
(第65回 日本輸血・細胞治療学会ポスター発表) - 組換えヒトアルブミンおよびCP-1 High Gradeを使用したヒト間葉系幹細胞の凍結保存
(第19回日本再生医療学会ポスター発表) - 牧野茂義,細胞凍害保護液CP-1 High Gradeの安全性と有効性
(第65回 日本輸血・細胞治療学会ポスター発表) - 牧野茂義,細胞凍害防止剤CP-1 High Gradeに期待すること, 医学のあゆみ, Vol273 No.3, 2020
FAQ
- Q1. CP-1® とCP-1® High Gradeの違いはなんでしょうか?
- Q2. どれくらいの期間、凍結保管できますか?
- Q3. 25%ヒト血清アルブミンの代わりに20%ヒト血清アルブミンを使用できますか?
- Q4. CP-1® High Gradeの保管温度は何℃ですか?
- Q5. 操作上の注意点は?
- Q6. 細胞懸濁液の調製には何を使用したらいいのか?
- Q7. 至適な細胞濃度(細胞密度)は?
- Q8. 細胞の凍結速度は?
- Q9. 造血幹細胞以外の細胞の凍結保存に関する情報は?
- Q10. 骨髄液の凍結保存はできますか?
- Q11. どのようにすれば購入できますか?
Q1. CP-1® とCP-1® High Gradeの違いはなんでしょうか?
組成や性能は変わりません。より安全性の高い原料への変更と製造場所(GMP対応施設)の変更となります。
Q2. どれくらいの期間、凍結保管できますか?
安定した条件であれば、-80℃でも1年程度は保管可能です。それ以上保管する場合は、液体窒素または-151℃を推奨します。
Q3. 25%ヒト血清アルブミンの代わりに20%ヒト血清アルブミンを使用できますか?
20%ヒト血清アルブミンもしくは自己血漿(凍結する細胞と同一由来の血漿)で代用することはできます。
これらを使用する場合にも、添加量は同量としてください。
Q4. CP-1® High Gradeの保管温度は何℃ですか?
2~30℃で保管してください。長期冷蔵保管をすると成分が析出する場合がありますので、長期冷蔵保管は避けてください。
Q5. 操作上の注意点は?
本品とヒト血清アルブミン(HSA)の混和時、およびHSA加本品と細胞懸濁液の混和時に発熱を伴う場合があります。
そのため、混和の際には氷上でおこなうか、あらかじめ冷やした本品を使用してください。また、HSA添加後は速やかに使用してください。
詳しい手順は使用説明書およびプロトコルをご確認ください。
Q6. 細胞懸濁液の調製には何を使用したらいいのか?
凍結保存する細胞の培養液(例:RPMI1640)、もしくは生理食塩水を用いて調製してください。
Q7. 至適な細胞密度(細胞濃度)は?
造血幹細胞を凍結保存する場合は、最終濃度1 x 108 cells/mL 程度に調製してください。
間葉系幹細胞を凍結保存する場合は、最終濃度1 x 106 cells/mL程度で保管した実績があります(実施例Ⅲ)。
Q8. 細胞の凍結速度は?
-2~-3℃/分程度が目安です。-5℃/分を超えないことが望ましいです。
Q9. 造血幹細胞以外の細胞の凍結保存に関する情報は?
ヒト骨髄由来およびヒト脂肪由来間葉系幹細胞を用いた凍結保存の検討結果を掲載中です。実施例Ⅲをご確認ください。
また、造血幹細胞以外の細胞における凍結保存方法は、プロトコルを参照ください。
Q10. 骨髄液の凍結保存はできますか?
骨髄液中の造血幹細胞を保存するといった目的であれば、原理的には使用可能ですが、赤血球と顆粒球の除去が必要です。
Q11. どのようにすれば購入できますか?
当社代理店からご購入いただけます。代理店については下記フォームよりお問い合わせください。
お問い合わせ
フォームが表示されるまでしばらくお待ち下さい。
恐れ入りますが、しばらくお待ちいただいてもフォームが表示されない場合は、こちらまでお問い合わせください。