リボテスト® レジオネラ
当ページは医療関係者の皆様を対象として作成しております。
尿中のレジオネラ・ニューモフィラ血清型 1LPS 抗原及びレジオネラ・ニューモフィラ L7/L12 抗原を検出するイムノクロマトキットです。
▼ 抗体技術(L7/L12)により菌固有の領域を識別します
▼ 判定時間は15分、初診時で検査結果が出ます
▼ レジオネラ・ニューモフィラ血清型1~15がすべて検出できます
| 統一商品コード | 製品名 | 包装・内容 | 詳細情報 |
| 551-45100-9 | リボテスト® レジオネラ | 10回用 | 【添付文書】 【リーフレット】 |
※L7/L12に対する抗体は旭化成株式会社が開発した技術です。「リボテスト」および「RIBOTEST」は旭化成株式会社の登録商標です。
製品コンセプト
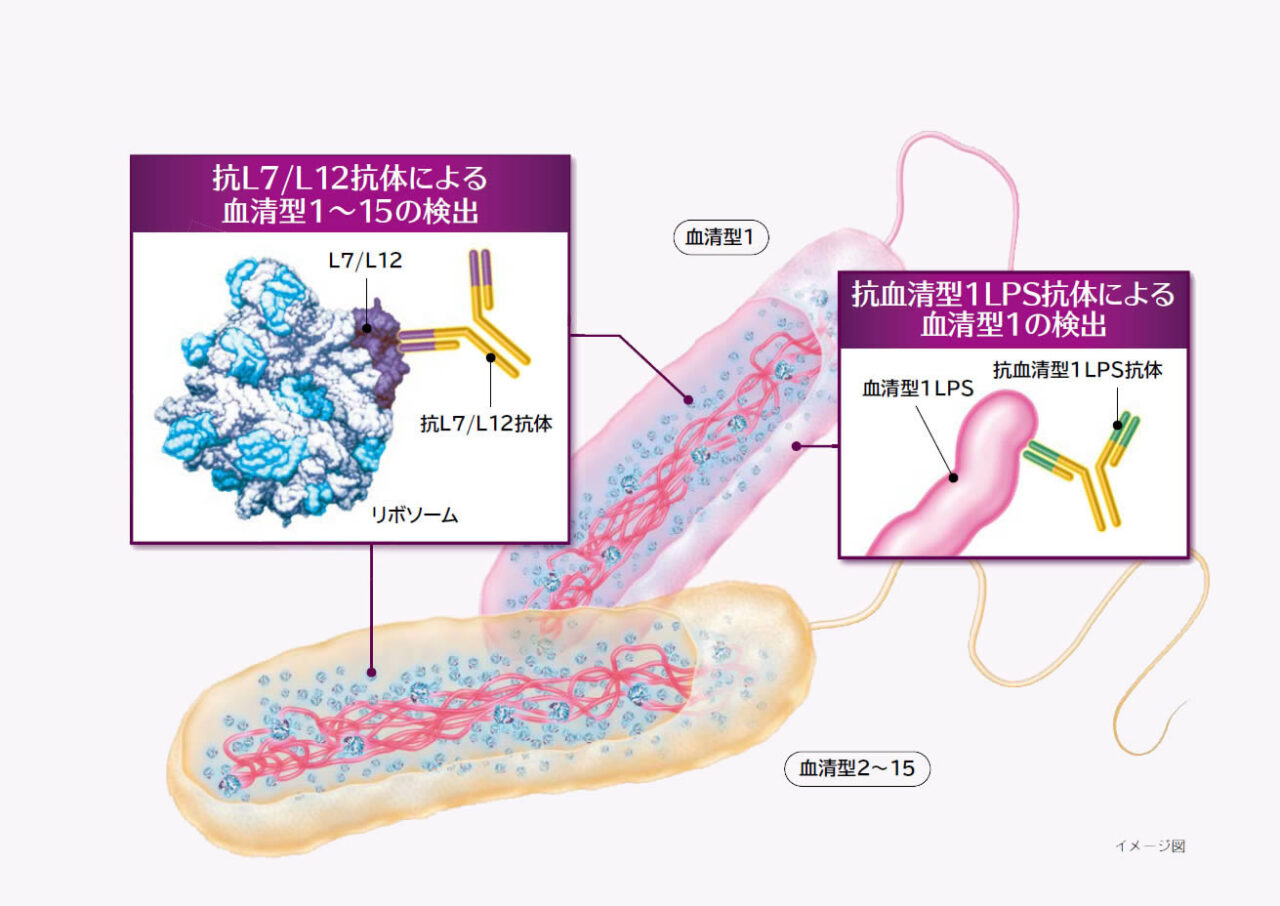
リボテスト® レジオネラは、レジオネラ・ニューモフィラ血清型1LPSを認識する抗血清型1LPS抗体に加え、レジオネラ・ニューモフィラのリボソームタンパク質L7/L12の菌固有領域を認識するモノクローナル抗体により、血清型にかかわらずレジオネラ・ニューモフィラの検出が可能となりました。
特徴
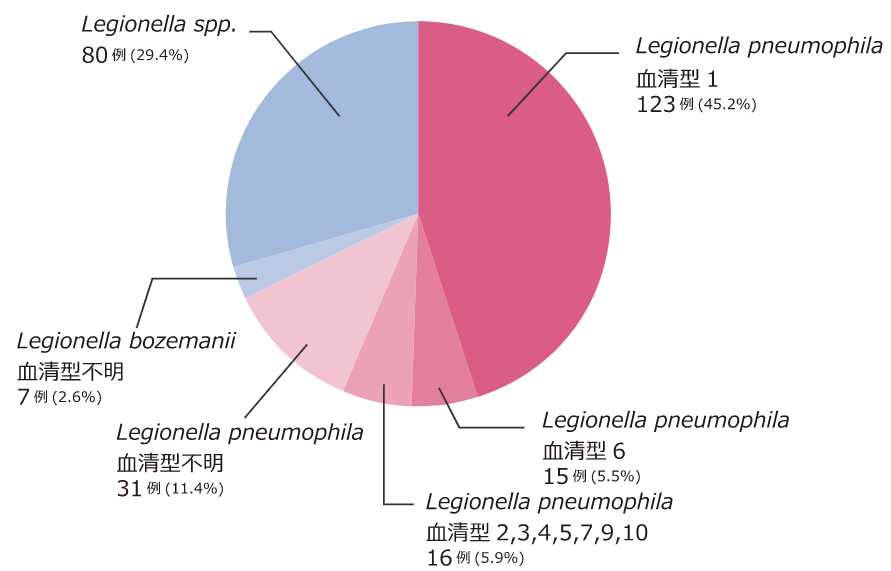
レジオネラ・ニューモフィラの血清型(1~15)がすべて検出できます。
レジオネラ肺炎の起因菌の多くは、レジオネラ・ニューモフィラであり、7割近くを占めています1)。 リボテスト® レジオネラは、レジオネラ・ニューモフィラのすべての血清型(1~15)を検出できます2)。
1)村上 日奈子. 臨床とウイルス., 2017; 45(3):82-86.
2)承認時評価資料
操作方法
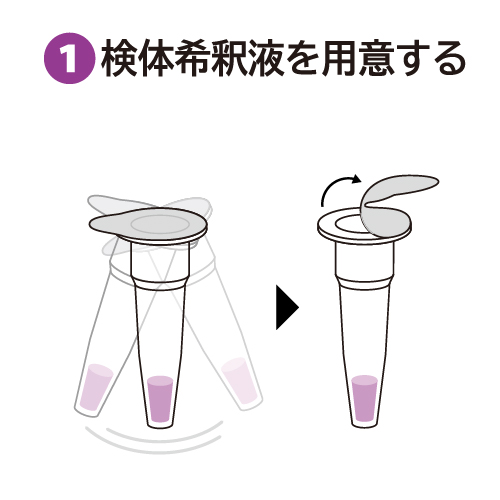
レジオネラ検体希釈液のチューブの蓋に付着している検体希釈液を振り落とし、蓋を取ります。
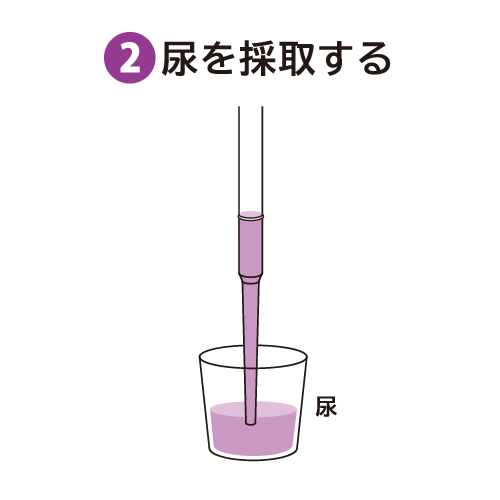
付属のスポイトを使用して0.5mLの目盛り線まで尿を吸い上げます。
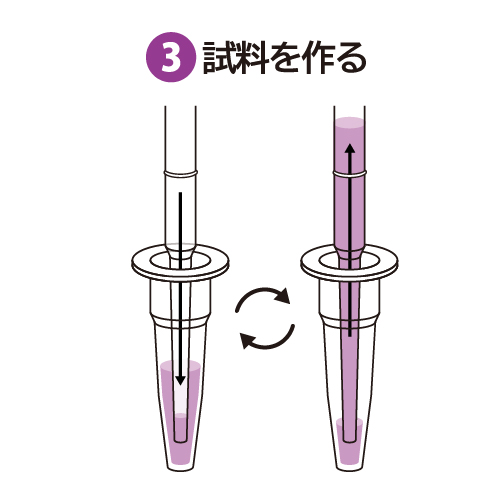
検体希釈液に2で採取した尿を全量滴下し、スポイトにて数回混和したものを試料とします。
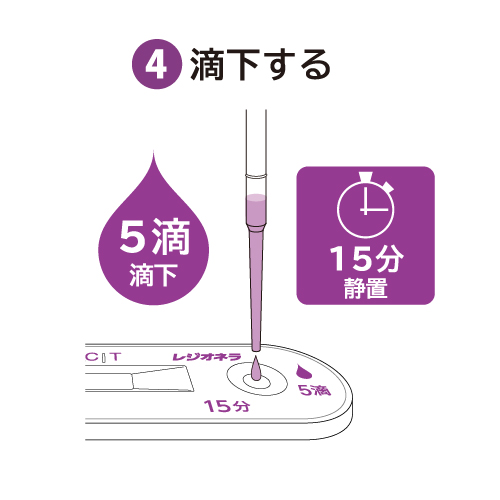
スポイトを使用して3で作った試料を0.5mLの目盛り線付近まで吸い上げ、テストプレートの試料滴下部に5滴滴下します。
15~30℃で15分間静置後、目視にて判定します。
※詳細は【添付文書】をご参照ください
判定方法

コントロールライン(C)とテストライン(T)の両方に赤紫色のラインが目視で確認できる場合は陽性と判定します。

コントロールライン(C)のみ目視で確認できる場合は陰性と判定します。

コントロールライン(C)が不明瞭、または確認できない場合は判定不能となります。
判定不能の場合は再度測定してください。
臨床成績
既承認品Aとの相関性
既承認品A(イムノクロマト法)
|
||||
陽性
|
陰性
|
合計 | ||
本キット |
陽性
|
49 |
5*2 |
54 |
陰性
|
2*1 |
45 |
47 |
|
| 合計 |
51 |
50 |
101 |
|
陽性一致率
|
96.1%(49/51) |
|||
陰性一致率
|
90.0%(49/50) |
|||
陽性陰性一致率
|
93.1%(94/101) |
|||
*1:既承認品A陽性、本キット陰性の2例は、培養法では2例とも陰性でした。
*2:既承認品A陰性、本キット陽性の5例は、培養法では4例が陽性、1例が陰性でした。
既承認品Bとの相関性
既承認品B(イムノクロマト法)
|
||||
陽性
|
陰性
|
合計 | ||
本キット |
陽性
|
49 |
5*4 |
54 |
陰性
|
1*3 |
46 |
47 |
|
| 合計 |
50 |
51 |
101 |
|
陽性一致率
|
98.0%(49/50) |
|||
陰性一致率
|
90.2%(46/51) |
|||
陽性陰性一致率
|
94.1%(95/101) |
|||
*3:既承認品B陽性、本キット陰性の1例は、培養法では陰性でした。
*4:既承認品B陰性、本キット陽性の5例は、培養法では4例が陽性、1例が陰性でした。
動画
リボテスト® レジオネラの紹介動画です。
